

高效液相色譜技術最早應用于藥物領域,包括效能/純度/性能分析、藥物(代謝)動力學/生物分析測試、純化、高通量篩選(HTS)、過程控制(IPC)監測和質量控制(QC)測試。制藥行業是HPLC的主要應用市場,同時也是HPLC向更高通量和更優性能發展的主要驅動力。本文簡要回顧了過去十年影響藥物分析發展的HPLC的重大進展。討論的主題如下,部分項目體現在一個典型的時間軸上,如圖1所示。
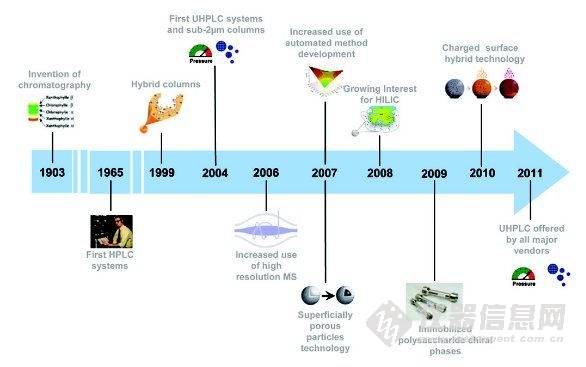
圖1 過去十年中影響藥物分析發展的HPLC技術進展(部分項目)
本文的目的是為繁忙的制藥科學家提供一個簡潔又全面的HPLC的重要的技術進展,每個主題都有實際使用過程中的便利和應用的簡短描述,從用戶的角度的評論,以及主要參考文獻(略)的支撐。
超高壓液相色譜(UHPLC)
UHPLC的革命性創新始于1997年James Jorgenson教授在概念驗證方面的研究,緊接著第一個商業化系統于2004年推出。今天,從HPLC到UHPLC的轉化大部分都是由主要制造商完成,這些制造商目前都可以供應某種類型的UHPLC產品。UHPLC系統、柱子以及應用的詳細綜述在其他地方都可以看到。UHPLC在藥物分析領域的基本原理、優勢、潛在的問題和最佳應用都有充分的文件記錄。
表1概述了UHPLC的突出特點和優勢。注意,較高的系統壓力允許使用更小的微粒填充的柱子(如亞2μm)得到更快的分析速度(圖2)或復雜樣品更出色的分離(圖3)。由于使用改良的進樣器,內徑較小的管路系統(< 0.005英寸),更小的紫外檢測器流動池(0.5 - 2μL),所有的UHPLC都有比較低的系統擴散(4σ時,~10-20μL)。比較典型的應用是內徑為2.1–3.0mm的柱子,填充物為亞2μm或亞3μm顆粒。其他重要的系統特征包括更小的系統死體積(0.1-0.3 mL)和更快的檢測器響應/數據采集速率(>40 pt/s),以實現高通量的應用。
表1 UHPLC的突出特點和優勢
|
UHPLC的系統特點 |
范圍和評論 |
|
最高壓力限制 |
15000到19000psi(1000到1250bar),流速2-5mL/min.兼容傳統的和亞-2微米顆粒的色譜柱。 |
|
低系統色散 |
根據儀器配置,儀器帶寬5-20μL(4σ),使用較小的連接管(<0.005"I.D)和小UV流通池(0.5-2μL),減小系統頻帶展寬。兼容ID低至2-3mm的色譜柱。 |
|
低的梯度保留體積 |
100-400μL(對于四元液相泵會更高),兼容高通量篩選(HTS)。小的保留(混合)體積可能影響UV檢測器噪聲。 |
|
其他 |
HTS快速的注射周期(-20s)和檢測響應,以及高的采集率(>40pt/t),兼容目前的HPLC方法需求(如流量范圍、柱溫箱尺寸、進樣環路) |
|
UHPLC的優勢 |
評論 |
|
高通量 |
在保持相似分辨率的情況下,與傳統的HPLC方法相比通量提高3-10倍。如純度分析5min(UHPLC)/20min(HPLC)。 |
|
快速方法開發 |
短色譜柱,快速分析是色譜柱和流動相快速篩選及方法優化的理想選擇。 |
|
高分辨 |
相對于HPLC,分辨率提高3倍,比如峰容量(Pc)400-600(HPLC為200) |
|
溶劑節省 |
分析時間短,使用較小ID的色譜柱,相比HPLC溶劑節省5-15倍。 |
|
高靈敏度 |
質量靈敏度增加3-10倍(樣品注入量減少)。長路徑UV流通池(50-60min)可以將濃度靈敏度提高6倍。 |
|
高精度 |
保留時間(2-3倍)和峰面積精密度(<1%RSD,進樣體積>1μL )顯著增加 |
|
可以與其他的方法聯用 |
UHPLC兼容高溫LC,2D-LC或者核殼色譜柱(單一或者組合聯用)。這些都是可選項,而不是“有它就不能有它”。 |
與傳統的HPLC相比,UHPLC具有分析速度快的優勢,圖2闡述了一種藥物分析由HPLC方法轉移為UHPLC方法的譜圖對比。從HPLC到UHPLC,根據幾何尺寸按比例縮放色譜柱及操作參數,可以在相同分辨率的情況下將分析時間減少10倍,這并不罕見。“保證好的分辨率的情況下進行更快的分析”這是大多數用戶考慮購買更昂貴的UHPLC設備的主要誘因。
UHPLC的另一個重要的好處是其對復雜樣品優秀的分離能力。這方面常常被忽視,在文獻中也很少報道。在合理的時間跨度(~1 h)內,400至1000范圍內的峰容量(PC)已經通過使用UHPLC來證實。峰容量是分辨率為1.0時,色譜圖上可以分辨的色譜峰個數;通常傳統的HPLC為200左右。有史以來第一次,UHPLC可以在單一維度,對復雜的藥品、天然材料、和其他困難樣品基質提供更有效的分析。圖3a和3b通過兩個應用 (植物提取物和胰蛋白酶的消化蛋白質)來說明Pc>300時,當前UHPLC的高分辨分離能力。
UHPLC的其他優勢包括溶劑節省(5-15倍),增強的質量靈敏度(3-10倍),以及在保留時間(2–3倍)和峰面積(<0.1%RSD)方面的卓越性能。注意,有關UHPLC中UV檢測靈敏度增加的報告往往會產生誤導,因為質量敏感度(分析物注入量)主要與柱的空隙體積有關。通常,UHPLC不會增加濃度靈敏度(最理想的一種靈敏度),因為我們不能希望使用小的流通池來增加信噪比,除非延長流通池的路徑長度 (如60毫米)。泵混合而導致的粘性發熱、基線擾動以及方法轉移等潛在問題已經有文獻描述,而且這些問題分別也是與特定的儀器相關聯的。一般來說,這些技術問題已經研究得比較清楚了,而且通過選擇合適的系統配置(如混合器體積)能夠很容易地減輕。但是, 由于培訓、與驗證數據系統的兼容性和其他方法轉移的問題,UHPLC在QC實驗室的應用仍然比較浪費時間。
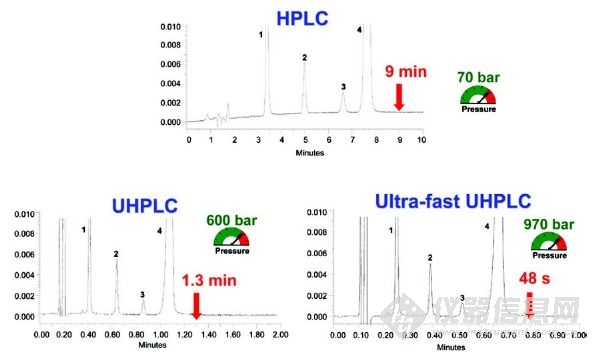
圖2 以商業制藥配方(Rapidocain) 質量控制分析為例:從傳統的HPLC到UHPLC使用幾何比例縮放。峰識別:1:對羥基苯甲酸甲酯,2:2、6-二甲基苯胺,3:尼泊金丙酯,4:利多卡因。HPLC條件:色譜柱RP18 150 x4.6毫米,5μm, F=1ml/min, Vinj=20μL。UHPLC條件: 色譜柱RP18 x2.1 50毫米,1.7μm,F = 600μL /min,Vinj = 1.4μL。超快UHPLC條件:色譜柱RP18 x2.1 50毫米,1.7μm,F = 1000μL /min,Vinj =1.4μL[16]。
我們經常聽到一些爭論,UHPLC也許并不需要,因為其他方法(高溫LC、核殼柱子或二維LC)可以更合算的提高速度或分辨率。這種推理并不是真實有根據的,因為與傳統的HPLC相比,UHPLC在使用過程會中可以與一個或多個以上的這些方法聯用獲得更出色的結果。這些方法都是可選項,而不是“有它就不能有它”。此外,“UHPLC”這個詞語可能在幾年內最終消失,因為所有新的HPLC都是UHPLC了。
HPLC色譜柱和固定相的發展
HPLC色譜柱是色譜系統的核心。在堿性分析物分析方面,制藥業一直是HPLC色譜柱向高速、高分辨率、更好的峰形發展的主要驅動力。此外,QC實驗室已經被要求改進色譜柱的批次重現性。從70年代到90年代,在填充材料的標準顆粒尺度(10-3μm)的逐級縮小方面已經有穩定的改進。80年代后期,高純度B型硅材料(低金屬含量)的引入是一個巨大進步,減少了硅醇的活性,并在批次間的一致性方面有重大改進。現在高純硅的使用是所有現代硅膠基質色譜柱的標準。
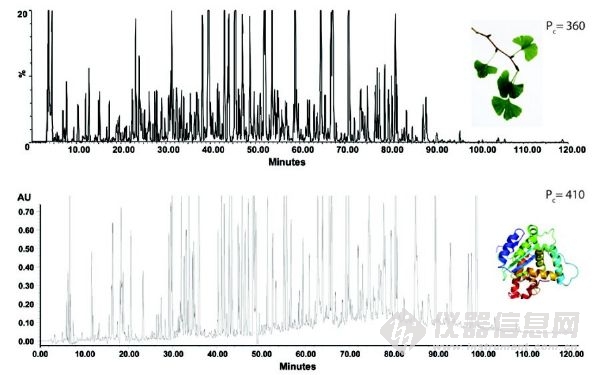
圖3 UHPLC 高分辨率分離(C18色譜柱,填充亞2μm顆粒)。(A)銀杏標準化提取物的色譜圖。梯度:5%到40%的乙腈,120分鐘,T=30°C, Lcol = 300mm,F = 0.2 mL/min,ΔPmax = 860 bar,峰容量可以達到360;(B)三種蛋白質的結合胰蛋白酶消化酶的色譜圖。梯度:5%到60%的乙腈,120min ,T=30°C,Lcol = 40cm,F = 0.16 mL/min,ΔPmax = 940bar,峰容量可以達到410。
HPLC色譜柱技術的近期進展已經被廣泛地綜述(已經有很多文獻綜述并討論了HPLC的色譜柱技術的近期進展)。表2總結了重大行業使用率較高的,用于提高生產力、穩定性、選擇性或保留時間(亞2μm,核殼粒子,混合物,新奇的鍵合反應,HILIC)或專業應用 (手性化合物或生物分子)的色譜柱。
表2 影響藥物分析的重要的HPLC色譜柱的研究進展
|
HPLC色譜柱重要研究進展 |
評論 |
|
亞2μm顆粒 |
全孔亞2μm顆粒產生較低的塔板高度和高的塔板效率。10多家供應商提供超過80種可用的化學反應,包括離子交換、尺寸排阻等。 |
|
亞3μm核殼顆粒 |
表面多孔型亞-3μm顆粒在低柱壓條件下提供改善的質量傳遞和較低的塔板高度。增加了在藥物分析中的使用案例。 |
|
混合硅顆粒 |
創新的顆粒提高色譜柱的化學穩定性(擴大pH范圍、溫度和壓力性能,親硅醇基活性) |
|
新奇的鍵合化學反應 |
多官能團的硅烷化學、極性嵌入式鍵合相、五氟苯酚(PFP)、 苯基-己基、表面帶電雜化(CSH)相,提供“正交”分離和增強的選擇性(與傳統的C18鍵合相相比) |
|
親水作用色譜(HILIC) |
反相色譜的“正交”分離對強極性化合物和次生代謝物有用 |
|
用于手性分離的多糖固定相 |
多糖手性固定相使得通常的色譜柱具有多用性和抗造性 |
|
生物分子色譜柱 |
創新的核殼結構和UHPLC大孔徑固定相可以有效改善蛋白質和治療性生物分子(如mAbs)的分析。 |
亞2 μm顆粒
1956年,Van Deemter就給出了使用非常小的顆粒進行快速、高效分離的預測。在過去五年中,典型填料的粒徑在不斷的減小,二十一世紀初,集中在亞2μm的硅微顆粒。正如預測的那樣,這些粒子(例如,1.7μm)產生卓越的性能(~ 280000 plates/m或~ 4μm/plate)。然而,填充亞2μm粒子的色譜柱產生高的背壓,通常填充內徑為2.1毫米,通過粘性發熱減少效率損失。對高壓力和低分散(減少附加柱的譜帶展寬)系統的要求導致了現代UHPLC系統的當前特點。進一步降低粒徑至小于1.5μm可能會產生更高的速度和性能。然而,它也必須伴隨著系統壓力的大幅增加和毛細管色譜柱內徑的減小。
核殼結構顆粒
Kirkland第一次描述了熔融的核或者核殼粒子的概念,減少質量轉移過程中的阻力。第一個核殼粒子具有如下特點:2.7μm表面多孔硅材料,無孔的核心(1.7μm),多孔的殼層(厚0.5μm)。這些亞3 μm的顆粒與亞2μm的完全多孔材料相比似乎具有相似的效率,但是可以產生更低的壓降。這種特殊的性能可能是由于殼體較短的擴散路徑,或者比較狹窄的填料分布。由于快速分離(HIS、IPC和清潔驗證)和在生物分子方面的應用,核殼色譜柱迅速獲得廣泛的接受。越來越多的制造商可以提供各種鍵合相和不同尺寸的粒子(1.3,1.7,2.6,1.3和5μm)。我們完全相信,與多孔微細顆粒的色譜柱相比,這些色譜柱在所有應用中具有很大的競爭力。
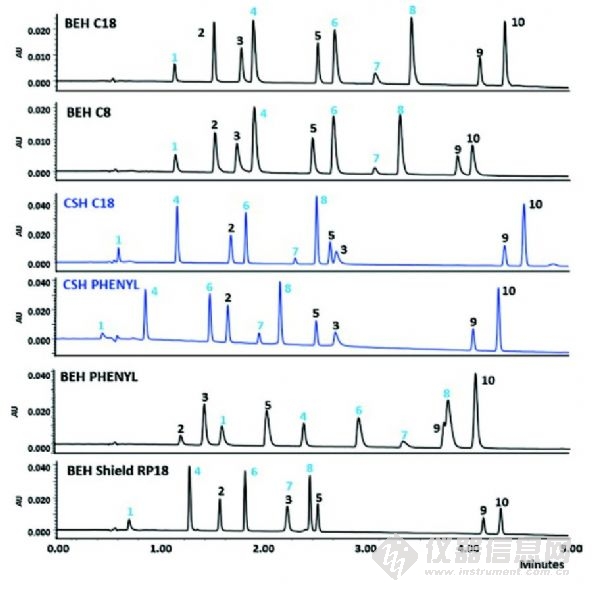
圖4 10種具有酸性、堿性和中性官能團的商品化藥物在BEH和CSH分析柱的分析比較,梯度洗脫,流動相含乙腈和0.1%的甲酸。峰1、4、6和8是基本藥物。從文獻中復印,已取得許可。
雜化
將有機基團引入到無機硅基體中形成雜交顆粒的理念在上世紀70年代首次由Unger提出,雖然第一根具有甲基基團的商業化的色譜柱在1999年才正式推出。這些混合物中的鍵合相被證明具有很好的pH穩定性(具有新奇的鍵合化學反應的pH范圍為1到12,而傳統的具有常規單功能鍵合硅顆粒的pH范圍為2-8),低的親硅羥基活性。2005年,引入第二代橋聯乙烯雜化 (BEH),并立即獲得了“主流”成功,特別是高pH值流動相以及UHPLC的應用方面。
新奇的鍵合反應
或許是因為批次之間重現性最好,傳統的單官能團的C18硅膠基質鍵合相仍是主要的產品,但是新的鍵合化學反應給困難的分離(極性嵌入式、苯基、己基苯基、含氰基的、戊烷氟苯基鍵合)帶來了更寬的pH值穩定范圍(多官能的硅烷化學鍵或異丙基保護的硅烷)和增強的選擇性。最近的一個創新方法稱為表面帶電雜化(CSH)技術,該項技術于2010年引入,由于在酸性,低離子強度流動相條件下,對高堿性分析物的峰形的改善,該項技術立即在藥物分析領域獲得了很好的接受度(如0.1%甲酸)。這項專有技術包括在固定相表面引入低水平的正電荷。這類似于早期在流動相中添加有機胺,如三乙胺,但由于離子抑制,已經不被LC/MS接受。圖4說明了與現在的鍵合相相比,CSH顆粒在峰形方面表現的優勢。注意,酸性化合物在CSH柱子上會有相對較高的保留,峰拖尾現象也會有所增加。
親水作用色譜(HILIC)
在反相LC(RPLC)條件下,若流動相中有機物含量比較低,就會導致相坍塌現象(鍵合相脫水),許多強極性化合物就無法獲得足夠的保留時間或者會存在問題。HILIC模式, 90年代由Alpert首次開發,使用親水固定相(硅、二醇、氰基、氨基、兩性離子的),類似RPLC使用的水緩沖和乙腈流動相,在極性藥物分析、輔助藥物代謝、氨基酸、多肽、神經遞質、低聚糖、碳水化合物、核苷酸或核苷方面的分析中越來越受歡迎。HILIC實際的保留機制可以認為是分析物分子“分區”到附著在親水結合基團的水層。與RPLC相比,HILIC其他突出的優勢包括“正交”選擇性(樣品制備兼容兩種模式),對質譜具有更高的電噴霧離子化靈敏度(5-15倍),較低的操作壓力。
固定化多糖手性固定相
成功包覆的多糖手性固定相(CSPs)的改進版本在2000年代末實現。與早期的CSPs具有相似的多功能,但是對于腐蝕性的溶劑具有更好的穩定性劑,可用于正相,極性有機和反相模式。
用于生物分子的色譜柱
80年代發展起來的大孔徑硅和聚合物填料可有效解決大型生物分子的分離。隨著重組蛋白,如單克隆抗體(mAb)等生物制藥的出現,質量控制中利用HPLC和毛細管電泳進行詳細表征的需求變得更加緊迫。最近,亞2μm微粒和核殼大孔徑顆粒以及一些創新的離子交換和尺寸排阻等材料也被證明可以有效的分離這些大分子的生物制劑。
高分辨率質譜(HRMS),電霧式檢測器(CAD)和自動方法開發系統(AMDS)
在過去十年中,其他具有高影響力的進展主要體現在HPLC檢測和自動化領域。
高分辨率質譜(HRMS)
HPLC與質譜的聯用(LC / MS),集合了HPLC的分離能力和質譜卓越的靈敏度和選擇性,已被視為完美的分析工具。LC/MS是雜質和降解鑒定,藥物研究中的高通量篩選技術(HTS),生物分析試驗(生物流體中藥物和代謝物的LC/MS/MS檢測),藥物合成工藝放大在線監測的首選技術。LC/MS已經成為高效藥物清潔驗證以及潛在的基因毒性雜質測定的標準技術平臺。過去十年中,HRMS(如TOF、OrbiTrap MS)和雜化質譜(如Quadrupole-TOF或ion trap-OrbiTrap)得到了快速發展。HRMS和UHPLC以及二維LC的聯用使得代謝組學、蛋白質組學, De Novo蛋白測序和生物制藥表征等領域的研究愈發活躍。新興的個性化醫療領域中生物標志物測定和疾病診斷的通用技術平臺也許是LC/MS最令人興奮的機會。
電霧式檢測器(CAD)
缺乏理想的通用檢測器常常被視為HPLC的局限,盡管UV/Vis檢測器可以檢測具有發色基團的化合物。示差折光檢測器不適合梯度洗脫,敏感性不夠。蒸發光散射檢測器(ELSD)使用噴霧器技術與激光光散射檢測,是HPLC的一個選擇,也可以兼容梯度洗脫,但最近已經被CAD(使用噴霧器和電暈放電檢測技術)超越,CAD可以提供更好的靈敏度(低至ng)和更好的線性。CAD正逐漸成為藥物化學中的HTS、反應過程監控以及原材料/輔料測試的主流的檢測器。
自動化HPLC方法體系(AMDS)
復雜混合物的HPLC方法開發是一個很耗時的工作,因為需要優化很多操作參數(柱尺寸,鍵合固定相和流動相A和B(有機溶劑/緩沖類型、pH值和離子強度)的類型,梯度洗脫時間和梯度范圍,柱溫度、流量)。一個常見的例子就是藥物活性成分(API)穩定性指示分析或純度測定,其中所有的雜質和降解產物必須分離,通過UV檢測器進行準確的定量。多年以來,基于模擬、預測、單純形優化、柱/流動相篩選的軟件或自動化系統已經促進HPLC方法的開發。雖然他們似乎還沒有很普及,但持續的改進提高了HPLC的性能和易用性。最新進入市場的是一個附加軟件包,兼容兩個常用的色譜數據系統。對于HPLC方法開發過程(優化)中最耗時的部分,該軟件利用用戶定義空間的自動化序列方法來解決,其中使用了實驗設計(DoE)和質量源于設計(QbD)的原則。導入完整的序列結果之后,該軟件還可以執行統計分析,并顯示最佳條件。圖5說明了應用在我們實驗室的該軟件的概念和特征。自DoE 和 QbD概念被接受以來,最初用戶表現出很高的興趣。AMDS對致力于早期藥物開發方法的實驗室特別有用。例如,為了支持利用多手性中心的復雜藥物分子進行API合成和藥物產品制造,10-20種具有代表性的HPLC方法(原材料、起始物料、中間體、最終的原料藥和藥物產品的非手性和手性方法,)接二連三地被開發出來。
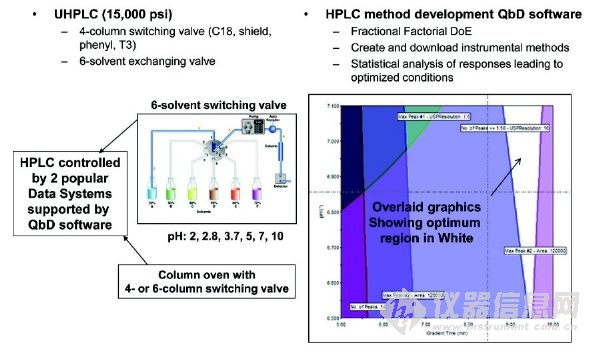
圖5 一個全自動方法開發系統的儀器構造圖解,該系統使用QbD軟件和所得結果的圖形,顯示最佳分離(白色)的操作范圍設計空間。
結論
總之, 最近幾年中,HPLC仍然是一個高度有活力的領域,在儀器、色譜柱技術、應用等方面有很多創新。醫藥科學家們最初將這些新技術應用于研究、開發和質量控制,他們是這項技術的早期采納者,同時也是受益者。UHPLC在研究與開發領域被快速的接受,并逐漸成為標準的UHPLC平臺,雖然在QC實驗室的應用速度慢一些。新的色譜柱技術可以更快和更有效的分析復雜樣品、手性分子和生物分子。最后,UHPLC和2-D LC與高分辨率質譜聯用技術的快速進展,已經徹底改變了生命科學的研究,并將會在臨床診斷方面產生更大的影響。這些進展得到了在快速發展的藥物開發領域工作的分析化學家的歡迎。
對于LC在接下來的幾年的發展前景,一些創新的工作已經被描述。就像Jim Jorgenson描述的:“更高的壓力(50000 psi)將使更小的顆粒和/或更長的色譜柱的使用成為可能,同時分離速度更快,效果也更好。由于熱量的產生和耗散問題,幾乎肯定的是需要使用sub-mm孔(毛細管)色譜柱。這并不是一件容易的事情,但是高速、高分辨率分離方面潛在的可能性是誘人的。”另外,在毛細管中填充極其均一的次微米二氧化硅粒子可以用來產生遠低于1μm的塔板高度,并能對蛋白質變異體進行令人印象深刻的分離。這兩個研究結果還沒有準備好馬上成為主流分析工作或QC,但是第一個結果是鼓舞人心的,因此在這里值得一提。
原文作者:Michael W. Dong, Ph.D.
Davy Guillarme, Ph.D.